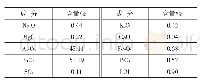
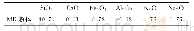《表2 高岭石布局数:煤灰中掺杂高岭土实验的量子化学研究》
采用量子化学计算软件对高岭石的微观结构进行计算分析,并通过图3体系总态密度图可以看到,费米能级(E=0)位于左侧的态密度范围内(HOMO),且左侧的电子态密度具有很高的峰值,而右侧(LUMO)距费米能级却较远,说明高岭石体系易于与电子接受体结合,而不易于与电子给予体结合。从图4中可以看出高岭石的最高占据轨道主要由氧原子贡献。因此当高岭石和电子接受体反应时,电子将从高岭石的氧原子上转移到电子接受体上,并与之成键。表2是高岭石的布局数表,从表中我们可以看到高岭石的O1、O2、O3、O4、O5、O6、O7、O8、O9、O10原子的净电荷分别为-0.982ev、-0.977ev、-0.975ev、-0.987ev、-0.984ev、-0.982ev、-0.977ev、-0.975ev、-0.983ev、-0.983ev,这些原子带的净电荷较多;O11、O12、O13、O14、O15、O16、O17、O18原子所带的净电荷为-0.791ev、-0.784ev、-0.784ev、-0.784ev、-0.784ev、-0.775ev、-0.791ev、-0.774ev。因此当高岭石与电子接受体发生反应时,Na+、Ca+等碱性氧化物中的亲电离子,会与高岭石中的组成HOMO的氧原子反应,使铝氧键断裂,与O1、O2、O3、O4、O5、O6、O7、O8、O9、O10原子结合形成新的化学键。
| 图表编号 | XD0010574900 严禁用于非法目的 |
|---|---|
| 绘制时间 | 2018.08.20 |
| 作者 | 杨政良、杜梅芳、陈义丽、李瑞莲、许鲁霞、李明强 |
| 绘制单位 | 上海理工大学理学院、上海理工大学理学院、上海理工大学理学院、上海理工大学理学院、上海理工大学理学院、上海理工大学能源与动力工程学院 |
| 更多格式 | 高清、无水印(增值服务) |
 提示:宽带有限、当前游客访问压缩模式
提示:宽带有限、当前游客访问压缩模式