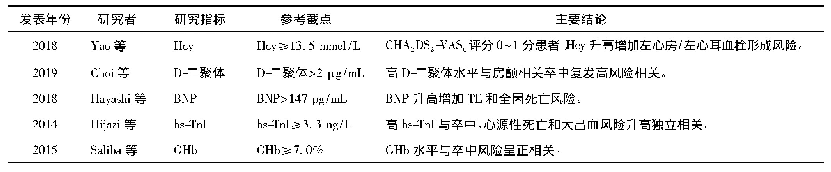
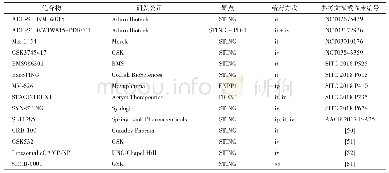
《表1 国外公司针对CD47治疗的临床前和临床研究状况》
 提示:宽带有限、当前游客访问压缩模式
提示:宽带有限、当前游客访问压缩模式
本系列图表出处文件名:随高清版一同展现
《抗CD47抗体、多肽类抗肿瘤药物专利发展状况分析》
2018年年中,Forty Seven公司在ASCO年会上公布了新型肿瘤免疫疗法Hu5F9-G4的2项独立临床试验的概念验证性数据。第一项Ⅰb/Ⅱ期临床试验在复发性/难治性非霍奇金淋巴瘤患者(r/r NHL)中,评估了Hu5F9-G4联合利妥昔单抗(rituximab)的疗效。在22例可评估患者中,客观缓解(ORR)率为50%,完全缓解(CR)率为36%。第二项Ⅰ期临床试验在晚期实体瘤患者中,评估了Hu5F9-G4的药动学(PK)和药效学(PD)特性。Hu5F9-G4为人源化抗CD47单克隆抗体,对应的临床前研究在WO2014/149477中提供,其公开了动物学相关实验,涉及安全性、药动学等。基于来自毒理学研究的结果,该专利申请表明非临床安全性评估程序支持针对所提出的临床试验应用Hu5F9-G4(例如静脉内输注)。Trillium公司的CD47抗体项目为SIRPαFc融合蛋白,与Hu5F9-G4具有相似的CD47亲和力(nmol·L-1级别)。SIRPαFc具有两大优势:首先,其相对分子质量更小(约80×103),相对于抗体分子的150×103具有更好的穿透性和组织分布性。其次,SIRPαFc对于红细胞的亲和力远低于Hu5F9-G4,表明其安全性可能更好。该抗体对应的专利申请为WO2014/094122,结果显示单结构域SIRPαFc对红细胞的结合性非常低,且CD47激动活性低。与其他CD47抑制剂相比,SIRPaFc具有更好的医疗用途。表1列出了现阶段国外公司针对CD47治疗的临床前以及临床研究状况,其中已经有5家公司进入临床阶段[4]。
| 图表编号 | XD0099624800 严禁用于非法目的 |
|---|---|
| 绘制时间 | 2019.10.15 |
| 作者 | 代月函、杨琳琳、靳春鹏、吕小蒙 |
| 绘制单位 | 国家知识产权局专利局专利审查协作北京中心、国家知识产权局专利局专利审查协作北京中心、国家知识产权局专利局专利审查协作北京中心、国家知识产权局专利局专利审查协作北京中心 |
| 更多格式 | 高清、无水印(增值服务) |