《表1 纳入研究基本信息》
 提示:宽带有限、当前游客访问压缩模式
提示:宽带有限、当前游客访问压缩模式
本系列图表出处文件名:随高清版一同展现
《骨肉瘤患者3种基因多态性与大剂量甲氨蝶呤不良反应相关性的Meta分析》
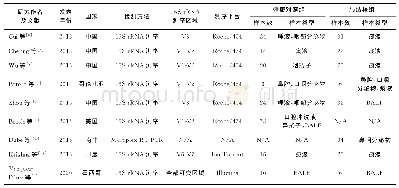
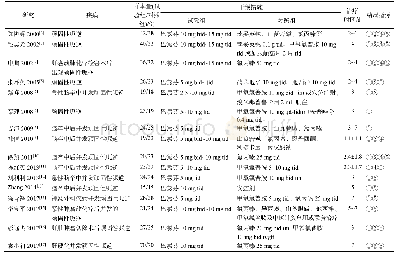
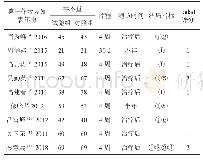
注:“NR”表示未报道;“A”表示MTHFR C677T;“B”表示MTHFR A1298C;“C”表示RFC1 G80A;“D”表示MDR1 C3435T;“#”表示ADR为G1-2;“*”表示ADR为G3-4
按照相应检索式进行检索,共检出文献1 901篇,手工补充纳入文献4篇,去重764篇,阅读题目和摘要后去除1 129篇,去除研究类型不符合2篇、研究人群不符合1篇、未报道结局指标数据1篇,最终纳入8篇(项)研究[10-11,16-21],其中4项研究[10-11,17-18]纳入Meta分析、4项研究[16,19-21]仅纳入描述性分析,合计608例患者。8项纳入研究中,3项研究[10,17,19]对象为亚洲人群,5项研究[11,16,18,20-21]对象为高加索人群,4项研究[11,16-17,21]纳入的患者为儿童,3项研究[10,19-20]同时纳入了儿童与成人,1项研究[18]未报道患者年龄范围。剂量方面,8项研究均严格限定为HD-MTX。基因多态性方面,研究MTHFR C677T、MTHFR A1298C、RFC1 G80A、MDR1 C3435T的研究数量分别为6[10-11,17-19,21]、5[17-21]、4[16-18,21]、2[16,20]项。经过χ2检验,8项纳入研究均符合HWE平衡。报道的结局指标包括血液毒性、肝毒性、肾毒性及口腔黏膜炎等不良反应,不良反应分级标准多为WHO标准或CTCAE。纳入研究基本信息见表1。
| 图表编号 | XD0083210600 严禁用于非法目的 |
|---|---|
| 绘制时间 | 2019.08.15 |
| 作者 | 宋再伟、刘爽、易湛苗、张恩瑶、赵荣生 |
| 绘制单位 | 北京大学第三医院药剂科、北京大学药学院药事管理与临床药学系、北京大学医学部药物评价中心、北京大学第三医院药剂科、北京大学药学院药事管理与临床药学系、北京大学医学部药物评价中心、北京大学第三医院药剂科、北京大学药学院药事管理与临床药学系、北京大学医学部药物评价中心、北京大学第三医院药剂科、北京大学第三医院药剂科、北京大学医学部药物评价中心 |
| 更多格式 | 高清、无水印(增值服务) |