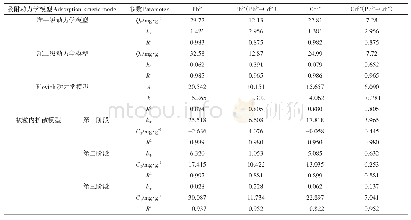
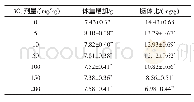
《表1 负载G-Rg3的纳米给药体系》
 提示:宽带有限、当前游客访问压缩模式
提示:宽带有限、当前游客访问压缩模式
本系列图表出处文件名:随高清版一同展现
《人参皂苷Rg_3对肿瘤的免疫调节作用及其纳米给药体系研究进展》
TF-转铁蛋白RGD-精氨酸-甘氨酸-天冬氨酸PTX-紫杉醇PLGA-聚乳酸-羟基乙酸共聚物PEG-聚乙二醇Glu-L-谷氨酸Phe-苯丙氨酸HSAMNP-人血清白蛋白磁性纳米颗粒BS-胆汁盐PC-磷脂酰胆碱MMS-混合胶束系统HACE-透明质酸-神经酰胺DSPE-二硬脂酰基磷脂酰乙醇胺EPC-卵磷脂酰胆碱
G-Rg3在恶性肿瘤的治疗中发挥重要的免疫调节作用,但是由于其水溶性较差,生物利用度较低,限制了临床应用。纳米技术的出现和发展成为解决这一问题的关键。将纳米级的高分子材料作为载体与难溶性的G-Rg3结合所形成的纳米给药体系能够有效地提高其水溶性。此外,相比于正常组织,肿瘤组织中的血管丰富,血管壁间隙较宽、结构完整性差,淋巴循环缺失,特定的大分子能够在肿瘤组织中富集、滞留,具有选择性的高通透和滞留效应(EPR)[39],使得纳米载药体系能够被动靶向肿瘤组织。在此基础上,引入能够特异性识别肿瘤组织的靶向配体对负载G-Rg3给药系统进行修饰,可以进一步赋予其主动靶向性。其中,研究较多的脂质体给药系统就是利用生物相容性较好的磷脂酰胆碱、胆固醇等脂质材料包裹G-Rg3并进行修饰而形成的,具有抑制肝癌、胃癌等多种实体瘤进展的效果,且不容易引起机体的免疫反应。纳米胶束则是依靠亲水性和疏水性共聚物的自组装形成“核-壳”结构包载G-Rg3,大大提高了G-Rg3的水溶性而且制备工艺简单。近年来,结合物理化学导向的靶向性技术,利用载体磁性、热敏、酸碱度敏感等特性制备而成的多种纳米颗粒,能够在外部环境改变时发生变化,缓慢释放药物,在提高G-Rg3溶解性的同时进一步增强对肿瘤细胞的杀伤作用,提高靶向的精确度,减少对于正常组织、器官的影响。总之,负载G-Rg3的纳米给药系统通常具有较小的直径,较高的表面反应活性、较强的吸附能力,较高的催化效率,较多的活性中心,能够大大增加药物稳定性、生物利用度、可降解性及靶向性[40],在G-Rg3的应用方面意义重大。本文梳理近10年有关负载G-Rg3纳米给药系统的研究进展,见表1。
| 图表编号 | XD0082037900 严禁用于非法目的 |
|---|---|
| 绘制时间 | 2019.08.12 |
| 作者 | 王曼、黄念、凌昌全 |
| 绘制单位 | 海军军医大学附属长海医院中医科、海军军医大学附属长海医院中医科、海军军医大学附属长海医院中医科 |
| 更多格式 | 高清、无水印(增值服务) |