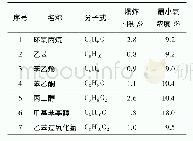
《表4 pH=2.2时沉淀重金属所需硫化物的理论最小浓度》
 提示:宽带有限、当前游客访问压缩模式
提示:宽带有限、当前游客访问压缩模式
本系列图表出处文件名:随高清版一同展现
《微生物硫氧化-硫还原回收垃圾焚烧飞灰中Cu和Zn》
注:pH=2.2时淋滤液中硫化物浓度实测为2.13 mg·L-1。
式中:[S2-]和[Zn2+]分别为淋滤液中S2-和Zn2+活度,活度系数根据Davies公式[18]计算;Ksp为溶度积常数。利用溶液中H2S的电离平衡(见式 (2)和式(3)) ,通过式(4)~式(6)可以计算出沉淀淋滤液中191 mg·L-1Zn2+所需最小理论硫化物浓度为9.14 mg·L-1,高于淋滤液中硫化物浓度,故Zn2+不会发生沉淀反应。计算所得Cd、Pb和Fe发生沉淀所需最小S2-浓度值均高于实验中淋滤液中硫化物浓度值(表4),故pH为2.2沉淀Cu时,Cd、Pb和Fe也不会发生沉淀。
| 图表编号 | XD0052049500 严禁用于非法目的 |
|---|---|
| 绘制时间 | 2019.05.26 |
| 作者 | 张瑞昌、邱会玲、王婷、冯帆、李梦婷 |
| 绘制单位 | 河南科技大学化工与制药学院、河南科技大学化工与制药学院、河南科技大学化工与制药学院、河南科技大学化工与制药学院、河南科技大学化工与制药学院 |
| 更多格式 | 高清、无水印(增值服务) |


![表1 土壤pH值与重金属浓度、综合污染指数与潜在生态风险指数[4]](http://bookimg.mtoou.info/tubiao/gif/WSWT202011031_15500.gif)

