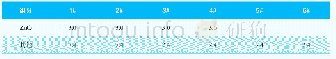
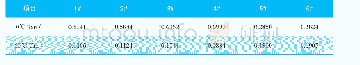
《表4 加料顺序对产物的影响》
CuSO4与Na2CO3的物质的量比为1∶1.2,反应温度75℃,用反滴法制备的产物生成速度快、数量多,混合之后立即生成暗绿色的碱式碳酸铜,正滴法制备反应结束时产物是蓝色的,随着沉淀时间的延长慢慢转变为暗绿色,5天后全都转变为暗绿色(见表4和图5)。正滴法制备时由于硫酸铜过量,生成的碱式碳酸铜不能溶解其中,因此反应一开始就有碱式碳酸铜从母液中析出,加上硫酸铜颗粒较大,不可避免会被包裹在产物中[5],反应结束后被包裹的硫酸铜慢慢从颗粒中释放出来,析出Cu4(SO4)(OH) 6·2H2O使沉淀呈蓝色[2]。反滴法制备由于碱式碳酸铜能溶于Na2CO3溶液形成铜络合物,反应初期只要有碱式碳酸铜生成就立刻溶于碳酸钠溶液形成铜的络合物,不会形成包裹物,只有当碳酸钠溶液对生成的碱式碳酸铜溶解达到饱和时,再滴入硫酸铜溶液时才有碱式碳酸铜颗粒开始析出。本实验的加料方法为反滴法。
| 图表编号 | XD0031126700 严禁用于非法目的 |
|---|---|
| 绘制时间 | 2019.02.18 |
| 作者 | 钟莲云、蒯洪湘、马少妹、白丽娟、曾俊杰、韦莹、韦晓、蓝平、廖安平 |
| 绘制单位 | 广西民族大学化学化工学院广西多糖材料与改性重点实验室培育基地、广西民族大学化学化工学院广西多糖材料与改性重点实验室培育基地、广西民族大学化学化工学院广西多糖材料与改性重点实验室培育基地、广西民族大学化学化工学院广西多糖材料与改性重点实验室培育基地、广西民族大学化学化工学院广西多糖材料与改性重点实验室培育基地、广西民族大学化学化工学院广西多糖材料与改性重点实验室培育基地、广西民族大学化学化工学院广西多糖材料与改性重点实验室培育基地、广西民族大学化学化工学院广西多糖材料与改性重点实验室培育基地、广西民族大学化 |
| 更多格式 | 高清、无水印(增值服务) |
 提示:宽带有限、当前游客访问压缩模式
提示:宽带有限、当前游客访问压缩模式