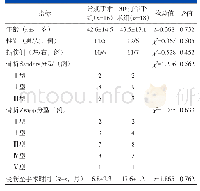
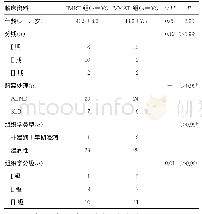
《表1 两组患者一般临床资料比较》
 提示:宽带有限、当前游客访问压缩模式
提示:宽带有限、当前游客访问压缩模式
本系列图表出处文件名:随高清版一同展现
《不同部位皮下注射硼替佐米联合治疗方案在初治不适合移植的多发性骨髓瘤患者中的安全性分析探究》
本研究经我院医学伦理委员会审核批准,前瞻性选取初诊不适合移植治疗的MM患者,纳入标准:(1)均符合国际骨髓瘤工作组(IMWG)多发性骨髓瘤的诊断标准(2014年更新版)[7],初次诊断为MM;(2)经至少2名专科医生同时确定为不适合移植治疗;(3)年龄>18岁;(4)根据《赫尔辛基宣言》(2013年版Fortaleza),均在知情下自愿签署知情同意书等相关协议。排除标准:(1)使用硼替佐米以外其他新药治疗者;(2)已接受1剂或多剂静脉注射硼替佐米治疗或者经静脉注射改为皮下注射硼替佐米治疗者;(3)不适合移植者,包括对本研究药物过敏者;或者伴其他恶性肿瘤、脑梗死、脑出血等严重疾病者;伴精神神经系统疾病(癫痫、痴呆、严重抑郁、躁狂、阿尔茨海默病等),不能配合治疗者;(4)依从性不佳,临床资料不全者;(5)拒绝接受本研究治疗方案者或同意本研究治疗方案但拒绝参与本研究者。最终纳入2019年5月~2020年3月间60例患者,采用随机数字表法将其分为两组,每组各30例,两组患者在性别、年龄、分型、RISS分期[8]等一般资料比较,差异无统计学意义(P>0.05),具有可比性,见表1。
| 图表编号 | XD00196872400 严禁用于非法目的 |
|---|---|
| 绘制时间 | 2020.12.25 |
| 作者 | 梁燕辉、沈孝春 |
| 绘制单位 | 广东省江门市中心医院血液内科、广东省江门市中心医院风湿免疫与介入科 |
| 更多格式 | 高清、无水印(增值服务) |