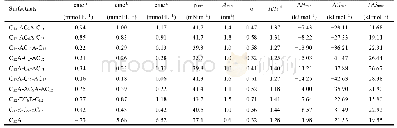
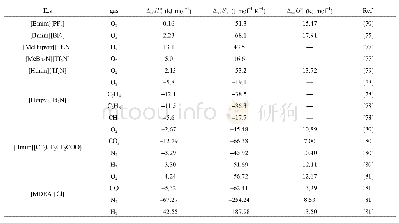
《表2 298.15 K和1.0 bar时CO、CO2在ILs中的热力学性质》
由于CO和CO2结构的不同,导致它们在常规ILs中的溶解行为也呈现出了一定的差异。下面以[Bmim][PF6]、[Bmim][MeSO4]和[Hmim][Tf2N]吸收CO[46-48]、CO2[54-56]行为为例进行比较分析。图3为373.15 K时CO、CO2在三种ILs中的溶解行为,由图3可知,CO2的溶解性能远高于CO,这可能是源于CO作为结构稳定的π酸配体,与ILs的作用弱于CO2;而且CO、CO2的溶解度均随压力的增加而线性增加,表明三种ILs均通过物理作用吸收CO和CO2;采用扩展型亨利定律对CO、CO2的溶解度与压力进行关联,利用获得的亨利系数得到了吸收过程中的ΔsolH m?、ΔsolSm?、ΔsolGm?、ΔsolC?p,m等热力学性质(表2)。从表2中可知,三种ILs吸收CO2的ΔsolGm?均小于CO,这表明上述ILs吸收CO2的自发性大于吸收CO的自发性;此外,三种ILs吸收CO2的ΔsolH m?均小于CO,表明ILs与CO2的相互作用大于ILs与CO的相互作用。
| 图表编号 | XD00118110600 严禁用于非法目的 |
|---|---|
| 绘制时间 | 2020.01.01 |
| 作者 | 刘佳佳、付雪、许映杰 |
| 绘制单位 | 绍兴文理学院化学化工学院、绍兴文理学院化学化工学院、绍兴文理学院化学化工学院 |
| 更多格式 | 高清、无水印(增值服务) |
 提示:宽带有限、当前游客访问压缩模式
提示:宽带有限、当前游客访问压缩模式