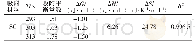《表2 Mg-HAP吸附Pb2+的热力学参数》
 提示:宽带有限、当前游客访问压缩模式
提示:宽带有限、当前游客访问压缩模式
本系列图表出处文件名:随高清版一同展现
《镁-钙羟基磷灰石吸附剂对水中Pb~(2+)的去除》
式中,T为绝对温度(K);KL为吸附过程完全平衡吸附常数(L·mol-1);R为理想气体常数[8.314J·(mol·K)-1];吸附焓和吸附熵可根据吸附常数KL随温度的变化对数据进行线性拟合.拟合结果如表2所示,计算得到的值均为负值,说明MgHAP对水中Pb2+的吸附过程是自发进行的.温度升高,吸附自发程度加大.吸附焓为正值说明MgHAP对水中Pb2+的吸附过程是吸热反应,温度升高有利于吸附反应的进行,进一步验证了Langmuir吸附等温模型得出的结论.吸附熵的值虽小但为正值,这表明Pb2+与Mg-HAP表面活性位点结合的过程中,会有不同类型的离子释放到液相中,这有可能使系统的粒子混乱程度增加从而导致熵增[17].由热力学函数ΔGθ=ΔHθ-TΔSθ<0可知,系统温度升高TΔSθ增大,ΔGθ则减小,这有利于Mg-HAP对Pb2+的吸附.
| 图表编号 | XD0064847500 严禁用于非法目的 |
|---|---|
| 绘制时间 | 2019.09.15 |
| 作者 | 何豪、朱宗强、刘杰、朱义年、阎起明、刘阳、莫南、玄惠灵、魏婉莹 |
| 绘制单位 | 桂林理工大学岩溶地区水污染控制与用水安全保障协同创新中心、桂林理工大学广西环境污染控制理论与技术重点实验室、桂林理工大学岩溶地区水污染控制与用水安全保障协同创新中心、桂林理工大学广西环境污染控制理论与技术重点实验室、桂林理工大学岩溶地区水污染控制与用水安全保障协同创新中心、桂林理工大学广西环境污染控制理论与技术重点实验室、桂林理工大学岩溶地区水污染控制与用水安全保障协同创新中心、桂林理工大学广西环境污染控制理论与技术重点实验室、桂林理工大学岩溶地区水污染控制与用水安全保障协同创新中心、桂林理工大学广西环境 |
| 更多格式 | 高清、无水印(增值服务) |