《表2 不同吸附体系H2O分子中各原子所带电量和释放电量》
e
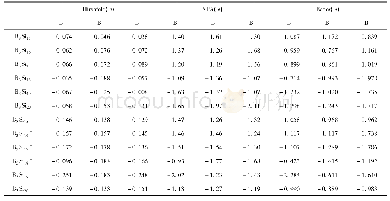
所建4种吸附模型的差分电荷密度图如图6所示。根据计算结果,在模型A1中,吸附H2O分子中H1和H2两个原子均带正电为0.50e,O原子带0.99e负电,此模型向基体释放电量较少,从吸附H2O分子向基体转移的电荷约为0.01e。在模型A2中,吸附H2O分子中H1和H2两个原子分别带正电为0.50e和0.49e,O原子带0.88e负电[24]。如表2所示,A2、A3和A4吸附模型中,吸附基体获得的电量分别约为0.11e,0.09e和0.12e,与模型A1相比,H2O分子吸附后向基体释放了更多的电荷,也说明A2、A3和A4吸附模型中H2O分子与基体之间产生了更强的相互作用。由此看出,H2O分子沿Y轴方向以H端吸附在Mo5+上方时,向基体释放的电量最小,也反映出该吸附模型中H2O分子与基体之间的相互作用较弱,与图5中模型A1的H2O分子DOS计算结果一致。
| 图表编号 | XD0043220800 严禁用于非法目的 |
|---|---|
| 绘制时间 | 2019.02.24 |
| 作者 | 杨树林、李姗、徐火希、兰智高 |
| 绘制单位 | 黄冈师范学院物理与电信学院、湖北大学物理与电子科学学院、黄冈师范学院物理与电信学院、黄冈师范学院物理与电信学院、黄冈师范学院物理与电信学院 |
| 更多格式 | 高清、无水印(增值服务) |
 提示:宽带有限、当前游客访问压缩模式
提示:宽带有限、当前游客访问压缩模式