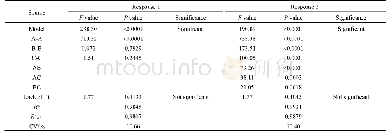
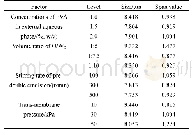
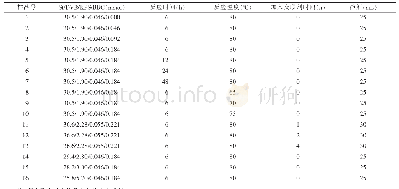
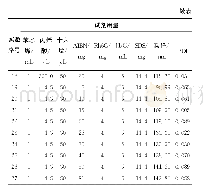
《表1 W/O/W溶剂挥发法制备亲水性小分子载药PLGA微球的文献》
 提示:宽带有限、当前游客访问压缩模式
提示:宽带有限、当前游客访问压缩模式
本系列图表出处文件名:随高清版一同展现
《基于响应面法对制备高包埋率ROP-PLGA微球的影响因素分析》
盐酸罗哌卡因(Ropivacaine Hydrochloride,ROP)是一种新型酰胺类局部麻醉药,通过作用于神经根和神经末梢的Na+通道,阻断痛觉神经冲动传导,从而可逆性地消除疼痛[1]。相比其他局麻药,ROP具有更低的心脏毒性和神经毒性,特别适用于术后疼痛管理[2-4]。但其半衰期短(t1/2=1.8 h),体内清除速率较快,单次注射的有效时间仅为2~4 h,必须频繁注射给药或通过导管持续灌注才能维持术后镇痛3~5 d效果[5]。前者会导致患者顺应性差,后者需要内置导管,也易造成组织感染及炎症等。因此,开发一种满足术后3~5 d镇痛管理需求的局麻药缓释剂型非常有意义[6-8]。微球(Microspheres,MS)缓释药物传递系统是将药物分子包裹于高分子聚合物中,采用特定技术制备成微球,以实现药物在体内长时间平稳释放。对于局麻药,微球缓释制剂可有效减少药物的血药浓度波动,从而减少神经毒性和心脏毒性[9-11]。聚乳酸-羟基乙酸共聚物[Poly(lactic-co-glycolic acid),PLGA]由乳酸和羟基乙酸聚合而成,由于其降解的终产物是二氧化碳和水,生物相容性优良,因此也是制备生物可降解高分子微球最常用的材料[12-14]。ROP作为一种亲水性小分子药物,可采用W1/O/W2复乳溶剂挥发法制备ROP载药微球。但制备过程中主要存在以下两方面的挑战:首先常规法一般采用机械搅拌或均质方法制备ROP-PLGA微球,导致制备的微球粒径分布较宽[15,16],而粒径不均不仅会影响药物的释放行为,也会影响制备批次重复性;其次是载药量及包埋率问题,由于盐酸罗哌卡因相对分子量极低,仅为311,在制备过程中药物分子极易扩散至外水相[17-20],因此导致此类亲水性的小分子药物的载药量及包埋率普遍偏低(表1)[15,16,21-23],不仅带来成本问题,而且会增加给药剂量,造成神经压迫和患者不适。
| 图表编号 | XD00198044000 严禁用于非法目的 |
|---|---|
| 绘制时间 | 2021.01.01 |
| 作者 | 文康、韦祎、马光辉 |
| 绘制单位 | 中国科学院过程工程研究所生化工程国家重点实验室、中国科学院大学化学工程学院、中国科学院过程工程研究所生化工程国家重点实验室、中国科学院过程工程研究所生化工程国家重点实验室、中国科学院大学化学工程学院 |
| 更多格式 | 高清、无水印(增值服务) |