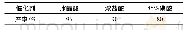《表1 催化剂种类对PET醇解反应的影响Tab.1 Effects of different catalysts on alcoholysis reaction of PET》
 提示:宽带有限、当前游客访问压缩模式
提示:宽带有限、当前游客访问压缩模式
本系列图表出处文件名:随高清版一同展现
《双酸型离子液体催化废PET醇解制备对苯二甲酸二丁酯研究》
注:反应条件为PET 10.0g,催化剂2.0g,正丁醇11.6g,反应时间8h,反应温度210℃.
由表1可见,采用传统催化剂时(实验2~5),PET醇解率均小于100%,且产物的收率也较低,表明PET未完全醇解.另外,采用传统催化剂时,后续催化剂的分离或去除相对复杂,尤其使用钛酸四丁酯或硫酸为催化剂时,需要耗用碱液并产生废水.当使用L酸性离子液体1-丁基-3-甲基咪唑氯铁酸盐[C4mim]Cl-FeCl3(x=0.67)(实验11) 或B酸性离子液体[HO3S-(CH2)3-mim]Cl(实验6)时,醇解反应几乎不能发生,PET醇解率和产物的收率非常低.同上述催化剂相比,B-L双酸型离子液体[HO3S-(CH2)3-mim]Cl-FeCl3(x=0.67)具有更佳的催化性能,PET醇解率为100%,产物DBTP和EG收率均超过97%(实验7).这可能是因为[HO3S-(CH2)3-mim]Cl-FeCl3(x=0.67)具有B和L双重酸性且两酸性位间兼有协同催化性能,该协同催化性能类似于双酸型分子筛催化剂[10].合成离子液体所用的金属氯化物的种类对醇解反应影响明显(实验7~10).催化剂[HO3S-(CH2)3-mim]Cl-FeCl3(x=0.67)显示了最佳的催化性能(实验7),而[HO3S-(CH2)3-mim]Cl-CuCl2(x=0.67)催化活性却非常差(实验10).上述结果的原因可能是因为合成离子液体所用的金属氯化物的L酸酸强度不同造成的,随着金属氯化物L酸酸强度的增加,所合成的离子液体酸强度随之增强[11].此外,与前期研究所用催化剂1-(3-磺酸)-丙基-3-乙基铵氯锌酸盐[HO3S-(CH2)3-NEt3]Cl-ZnCl2(x=0.67)催化剂[12]相比(实验12),离子液体[HO3S-(CH2)3-mim]Cl-FeCl3(x=0.67)因其结构含有芳香环而具有更佳的热稳定性,且产物收率更高.
| 图表编号 | XD0015364400 严禁用于非法目的 |
|---|---|
| 绘制时间 | 2018.07.01 |
| 作者 | 李海燕、刘仕伟、于世涛 |
| 绘制单位 | 青岛科技大学化工学院、青岛科技大学化工学院、江苏省生物质能源与材料重点实验室、青岛科技大学化工学院 |
| 更多格式 | 高清、无水印(增值服务) |