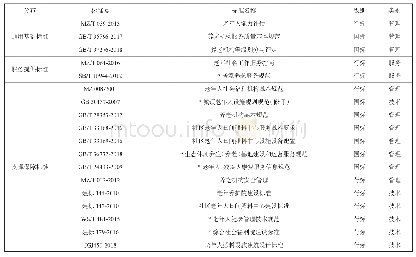
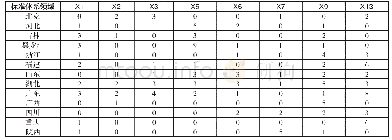
《表1.分子诊断领域试剂产品国家行业标准》
适用于荧光PCR法的行标主要为YY/T 1226-2014《人乳头瘤病毒核酸(分型)检测试剂(盒)》(4.1项)、YY/T1256-2015《解脲脲原体核酸扩增检测试剂盒》、YY/T 1424-2016《沙眼衣原体DNA检测试剂盒(荧光PCR法)》、YY/T1462-2016《甲型H1N1流感病毒RNA检测试剂盒(荧光PCR法)》、YY/T 1591-2017《人类EGFR基因突变检测试剂盒》、YY/T 1586-2018《肿瘤个体化治疗相关基因突变检测试剂盒(荧光PCR法)》等。总结这几年涉及荧光PCR法的行业推荐性标准不难发现,对于荧光PCR法产品的质量控制主要检测以下几个项目:外观、准确性(阳性符合率)、特异性(阴性符合率)、重复性(精密度)、检测限(检出限、最低检测限)、核酸提取效率、稳定性等,个别具有不同基因分型的产品需要进行基因分型检测。荧光PCR方法产品较为多样化,常见产品可以测试多种基因分型,为合理科学判定产品的质量,检测项目在选用检测样本时应考虑分型的因素,如YY/T 1226-2014规定重复性至少用两种不同型别国家分型参考品或经标化的企业参考品进行检测,YY/T 1527-2017规定重复性样品α-非缺失型地中海贫血基因型不少于2个、α-缺失型地中海贫血基因型不少于3个、β-地中海贫血基因型不少于5个等。并且,在最新发布的三项标准YY/T1591-2017(2017-12-05发布)、YY/T 1596-2017(2017-12-05发布)、YY/T 1586-2018(2018-02-24发布)对各项重要指标的参考品设置均提出了要求,这一项变化更有利于规范不同检测机构、企业在对产品质量检测,有助于增加检测结果的一致性和互通性,统一对产品的质量评价。
| 图表编号 | XD0082759900 严禁用于非法目的 |
|---|---|
| 绘制时间 | 2019.07.15 |
| 作者 | 刘倩瑜、吴静标 |
| 绘制单位 | 广东省医疗器械质量监督检验所、广东省医疗器械质量监督检验所 |
| 更多格式 | 高清、无水印(增值服务) |
 提示:宽带有限、当前游客访问压缩模式
提示:宽带有限、当前游客访问压缩模式