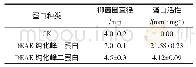
《表1 两种蛋白亚型的纯化表》
将Sephadex G-50第二峰进行DEAE-Sepharose弱阴离子交换层析,分别收集穿透峰1(67–82管,C1)和穿透峰2(88–121管,C2),其色谱结果和PAGE分析结果如图2所示。由图2B可知,DEAE-Sepharose可将PAGE上对应的两种蛋白分离开,穿透峰1(C1)和穿透峰2(C2)均为PAGE纯的蛋白,将其分别命名为ASPR-C-1和ASPR-C-2。为进一步验证其纯度,分别取两个峰的组分进行SDS-PAGE分析,结果如图3A所示,由图可知,ASPR-C-1(泳道1)和ASPR-C-2(泳道2)在还原条件下为SDS-PAGE纯的组分。两种蛋白的纯化过程如表1所示,ASPR-C-1比活力为73.69 U/mg,纯化倍数为5.35,ASPR-C-2酶的比活力为146.68 U/mg,纯化倍数为10.64。
| 图表编号 | XD0040386000 严禁用于非法目的 |
|---|---|
| 绘制时间 | 2019.01.25 |
| 作者 | 王香玲、李娴、何火聪、李玲玲、吕迪、陈翠煌、叶小强、刘树滔、潘剑茹 |
| 绘制单位 | 福州大学生物科学与工程学院、福州大学生物科学与工程学院、福建医科大学附属肿瘤医院、福建省肿瘤医院放射生物学及肿瘤放射治疗学研究室、福建省科技厅转化医学重点实验室、福州大学生物科学与工程学院、福州大学生物科学与工程学院、福州大学生物科学与工程学院、福州大学生物科学与工程学院、福州大学生物科学与工程学院、福州大学生物科学与工程学院 |
| 更多格式 | 高清、无水印(增值服务) |
 提示:宽带有限、当前游客访问压缩模式
提示:宽带有限、当前游客访问压缩模式