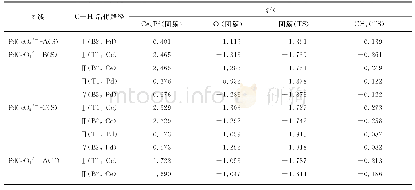
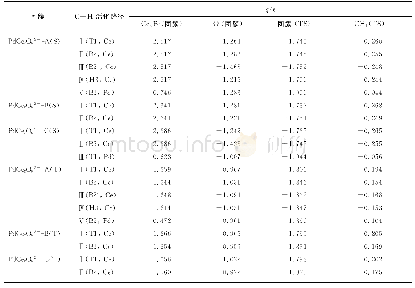
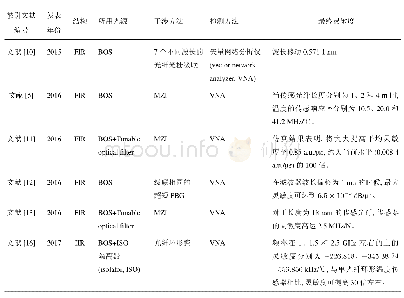
《表1 NBO计算的一些重要原子的自然密度》
 提示:宽带有限、当前游客访问压缩模式
提示:宽带有限、当前游客访问压缩模式
本系列图表出处文件名:随高清版一同展现
《无氧/低氧环境中zigzag型焦炭N的迁移转化特性》
R1到IM1为六元吡啶环的开环过程,由R1的M ulliken布居电荷分布(见图5(a))可知,N3原子和C2原子表现为作用引力,键能较大,致使吡啶环中C2-N3键断裂需翻越237.4 kJ/mol的能垒,表明N原子的剥离在热力学上较难进行,为整个反应的限速步之一。伴随着吡啶环的开环,N3-C4-C5组成的闭三元环形成,其原因可由布居电荷分析,N3-C4键的断裂改变了布居电荷在焦炭表面的分布,结合图5(a)、图5(b)和5(c)可知,C5原子表面负电荷逐渐减少正电荷逐渐增加,使得C5和N3原子间作用引力逐渐增强,促使C5-N3键键合,电荷转移是该闭环形成的原因之一。随着C2和C4原子的逐渐靠近(0.296 nm(IM1)到0.215 nm(TS2)再到0.150 nm(IM2)),C2和C4原子间作用力逐渐增强,N3和C4间结合能逐渐减弱,使得C2-C4发生键和,N3-C4键发生断裂。IM1需克服84.92 kJ/mol的能垒经TS2生成中间体IM2。IM2到IM3表现为N原子的迁移过程,伴随着N原子的迁移,C7原子供体向N3原子受体提供电子,促进两者原子间键合,过程仅需克服4.2 k J/mol的能垒,同时放出120.67 kJ/mol的热量,表明IM3较稳定,可在体系内存在较长时间。随后为NO在IM3表面的吸附过程,NO以N-down的形式吸附在N原子表面形成中间体IM4,过程无需克服能垒并放出260.01 k J/mol的高热量,为后续反应提供热驱动力。IM4→IM5为氧原子的迁移过程,该过程可由电子转移进行分析。由自然群体密度(见表1)计算结果可知,C7原子的价电子从1.90433(在IM4中)下降到1.81130(在IM5中),而O9原子的价电子从3.18171(在IM4中)增加到3.20406(在IM5中),表明氧迁移过程中C7可以向受体O9提供电子,增强C7和O9原子间结合力,促使C7-O9键合;此外,N3原子的价电子从2.60384(在IM4中)下降到2.54506(在IM5中),而N8原子的价电子从2.35500(在IM4中)增加到2.40173(在IM5中),表明N3原子表面负电荷密度降低,N8原子表面负电荷密度增大,N3将部分电子转移到N8原子表面,使得N3-N8间键能增大。进一步分析表1可知,N8-O9在IM4中表现为作用引力,使得N8-O9键断裂需翻越130.92 k J/mol的能垒,而IM5较IM4的位置低304.7 k J/mol(见图4),可知氧原子迁移为高放热过程,在热力学上更容易发生,并且形成的中间体IM5较IM4更稳定。随后N8原子绕N3-C5轴旋转形成IM6,最后为N2在焦炭表面的解吸过程,过程需克服142.25 kJ/mol能垒才可发生。
| 图表编号 | XD00153573100 严禁用于非法目的 |
|---|---|
| 绘制时间 | 2020.08.01 |
| 作者 | 陈萍、李计划、顾明言、陈光 |
| 绘制单位 | 安徽工业大学能源与环境学院、安徽工业大学能源与环境学院、安徽工业大学能源与环境学院、安徽工业大学能源与环境学院 |
| 更多格式 | 高清、无水印(增值服务) |