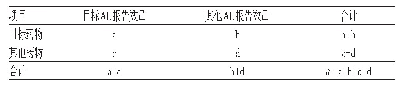
《表1 美国FDA数据库28件助听器不良事件》
以医疗器械不良事件监测为例,在我国主要由监测机构负责对报告进行收集,并在体系内进行封闭式评价和消化,缺少生产企业的参与[7]。而药监局官网没有具体企业及产品的相关风险信息情况或不良事件查询端口,医疗机构、生产企业和患者不能有效利用这些监管资源,难以形成正面反馈。而欧美、日本等国家已经形成较完善不良事件监测机制。笔者通过查询美国FDA不良事件数据库,选取2014年-2018年涉及助听器不良事件中28件进行了整理,暴露出儿童吞咽电池、过敏、电池寿命问题等9种问题,见表1。
| 图表编号 | XD0087850700 严禁用于非法目的 |
|---|---|
| 绘制时间 | 2019.03.30 |
| 作者 | 牛帅、塔娜、王晓玲 |
| 绘制单位 | 上海市食品药品监督管理局认证审评中心、国家药品监督管理局医疗器械技术审评中心、上海市食品药品监督管理局认证审评中心 |
| 更多格式 | 高清、无水印(增值服务) |
 提示:宽带有限、当前游客访问压缩模式
提示:宽带有限、当前游客访问压缩模式