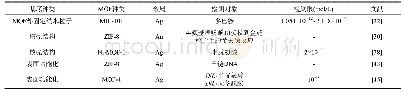
《表1 基于异肽键连接的分子粘合剂的应用》
超强分子粘合剂由于其特异性、稳定性且反应快速的优势,为蛋白质环化开辟了新思路。近年来,利用异肽键介导的分子粘合剂对蛋白质进行分子修饰,取得了较大进展(表1)。2015年,Schoene等[9]将SnoopTag/SnoopCatcher和isopeptag/pilin-C系统应用于β-内酰胺酶的分子环化,发现野生酶在55℃条件下发生聚沉、可溶性蛋白显著减少,导致活性快速丧失,而环化蛋白活性则几乎不受影响。差示扫描量热法(Differential scanning calorimetry)分析线性和环化蛋白的溶解温度,与线性蛋白相比,环化蛋白的Tm值显著上升。野生植酸酶在55℃以上的环境中加热10 min可溶性蛋白活性开始降低,而SpyTag/SpyCatcher环化的植酸酶在90℃才开始略微下降,且活性影响较小。圆二色谱(Circular dichroism)检测结果显示,与野生型植酸酶相比,环化后的植酸酶二级结构稳定性显著增加。Wang等[30]将SpyTag/SpyCatcher用于介导地衣聚糖酶的环化,经热处理后,环化蛋白的活性显著高于线性蛋白。此外,有研究发现SpyTag/SpyCatcher环化增强了萤火虫荧光素酶的热稳定性,同时其生物活性不受影响[32]。以上各研究团队的结果可以得出同样的结论,即环化后蛋白的热稳定性、抗逆能力显著提高。
| 图表编号 | XD0040389300 严禁用于非法目的 |
|---|---|
| 绘制时间 | 2019.04.25 |
| 作者 | 高德英、曹佳雯、孙小宝、周可鑫、张铁涛、王谦 |
| 绘制单位 | 浙江万里学院生物与环境学院、浙江万里学院生物与环境学院、浙江大学动物科学学院、浙江万里学院生物与环境学院、浙江万里学院生物与环境学院、中国农业科学院特产研究所、浙江万里学院生物与环境学院 |
| 更多格式 | 高清、无水印(增值服务) |
 提示:宽带有限、当前游客访问压缩模式
提示:宽带有限、当前游客访问压缩模式