《表1 配合物1~3在氮气氛围的DMF溶液中的电化学性质》
配合物1~3的合成步骤如图1所示.通过质谱和元素分析确认每个配合物的结构和纯度,其结果与文献[17]的数据相一致.所有的电化学测试均在CHI660E电化学工作站上进行.首先研究配合物在惰性气体氮气氛围中的电化学性质,将配合物溶于除水的DMF溶剂中(浓度为1.0 mmol?L-1),溶液通氮气后采用三电极体系记录循环伏安曲线,如图2(a)所示.在电势范围0至-2.0 V内,配合物2在-1.10 V处有1个可逆的还原峰;在-1.60 V和-1.80 V处有2个不可逆的还原峰;在-1.10 V处的可逆峰所对应的电流密度与扫描速率的平方根成线性关系,说明该过程是扩散控制过程(图3),该峰归属于CoII/I氧化还原过程.其余2个不可逆的还原峰则来自于配体,分别对应于2个亚胺键的还原反应[18].据表1,相比于配合物2,配合物1的3个还原峰均向正方向移动,其主要原因是配合物1上带有吸电子基团(-F),会导致其最高占有分子轨道(HOMO)和最低未占用分子轨道(LUMO)之间的能隙减小.
| 图表编号 | XD0038129600 严禁用于非法目的 |
|---|---|
| 绘制时间 | 2019.05.10 |
| 作者 | 周倩倩、黎挺挺、郑岳青 |
| 绘制单位 | 宁波大学应用固体化学研究中心、宁波大学应用固体化学研究中心、宁波大学应用固体化学研究中心 |
| 更多格式 | 高清、无水印(增值服务) |
 提示:宽带有限、当前游客访问压缩模式
提示:宽带有限、当前游客访问压缩模式
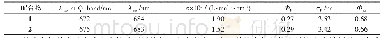


![表3 配合物[(btp)Pt(ipap)]Cl与(btp)Pt(mpmt)Cl的电化学性质](http://bookimg.mtoou.info/tubiao/gif/WJHX202101004_04300.gif)

