《表1 青光眼RGC程序性坏死的主要影响因素及相关分子》
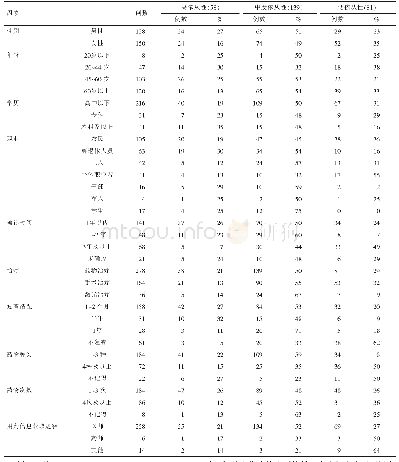
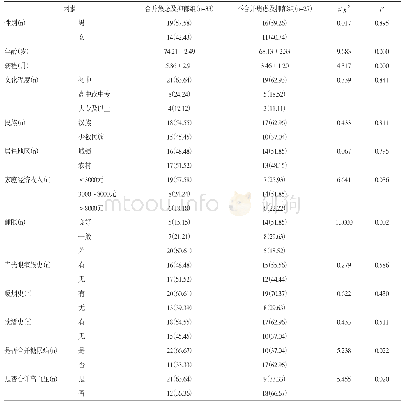
研究发现,在高眼压条件下小鼠RGC-5细胞的RIP3表达水平明显升高,而敲除RIP3基因后其丙二醛(malondialdehyde,MDA)表达水平和糖原磷酸化酶(glycogen phosphorylase,PYGL)活性显著降低,提示RIP3可能通过诱导PYGL活性和促进活性氧族(reactive oxygen species,ROS)累积介导RGC的程序性坏死[13]。PYGL是糖原分解的关键酶,RIP3可能通过激活PYGL增加能量代谢,调节TNF诱导的ROS生成,促进细胞坏死[14]。另有研究指出,在静水压升高后RGC-5细胞中RIP3和MLKL的表达及磷酸化水平均明显升高,且细胞内Ca2+浓度升高,坏死的RGC数量增加,提示MLKL可能参与了RGC的程序性坏死并与胞内Ca2+浓度增加相关[15]。有研究进一步提出MLKL可能以瞬时受体电位通道7(transient receptor potential melastatin related 7,TRPM7)为靶点介导Ca2+内流,参与程序性坏死时的质膜破裂[16]。也有研究报道在NIH3T3细胞程序性坏死中未能发现大量Ca2+内流和TRPM7通道的作用,认为Ca2+信号与程序性坏死相关性不大[17]。关于MLKL通过质膜定位靶向调控TRPM7通道介导程序性坏死的观点尚存在争议,仍需进一步研究。青光眼RGC程序性坏死的主要影响因素及相关分子见表1。
| 图表编号 | XD00216857500 严禁用于非法目的 |
|---|---|
| 绘制时间 | 2021.03.01 |
| 作者 | 赵文娟、范春玲、洪俊、何烨、胡熙敏、张齐、熊鲲 |
| 绘制单位 | 中南大学基础医学院人体解剖学与神经生物学系、中南大学基础医学院人体解剖学与神经生物学系、中南大学基础医学院人体解剖学与神经生物学系、中南大学爱尔眼科学院、中南大学湘雅医学院、中南大学基础医学院人体解剖学与神经生物学系、中南大学基础医学院人体解剖学与神经生物学系 |
| 更多格式 | 高清、无水印(增值服务) |
 提示:宽带有限、当前游客访问压缩模式
提示:宽带有限、当前游客访问压缩模式