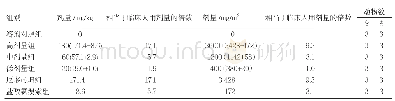
《表1 各国异常毒性检查的试验设计》
异常毒性检查用于检测生物制品中外源污染物,在以往各版《欧洲药典》和WHO生物制品技术指南文件中均有规定,WHO称为无害试验(innocuity test)或异常毒性试验(test for abnormal toxicity)[1],《美国药典》34称为一般安全性试验(general safety test)[2],《中国药典》三部(2015版)及《欧洲药典》7.0均称为异常毒性检查(abnormal toxicity test)[3-4]。各国及WHO标准中异常毒性检查方法见表1,尽管在不同国家该项检查的名称略有不同,但除《中国药典》三部(2015版)设有动物空白对照、WHO不允许复试外,异常毒性检查方法基本相同。
| 图表编号 | XD00171479700 严禁用于非法目的 |
|---|---|
| 绘制时间 | 2020.06.20 |
| 作者 | 王晓娟、赵勇、曹琰、郭中平 |
| 绘制单位 | 国家药典委员会、中国医学科学院医学生物学研究所、国家药典委员会、国家药典委员会 |
| 更多格式 | 高清、无水印(增值服务) |
 提示:宽带有限、当前游客访问压缩模式
提示:宽带有限、当前游客访问压缩模式