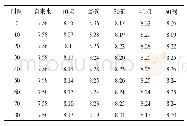
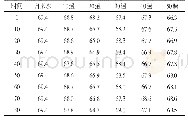
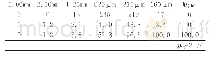《表1 壳聚糖(1.0 g/L)分子量随时间的变化规律(50℃、1.5%H2O2)》
Chang等[23]发现过氧化氢降解的壳聚糖分子量符合一级动力学,并且降解速率比超声降解快很多,而与壳聚糖酶降解速率相当,分子量变化如表1;痕量的过渡金属和壳聚糖结构中的氨基对β-1,4糖苷键的断裂有很大的影响。Qin等[22]研究了H2O2对壳聚糖的降解,发现均相反应降解的壳聚糖的分子量成单模态分布,而非均相的成双峰态分布;分子量随反应温度、反应时间和过氧化氢浓度的增大均降低;低浓度的酸可以促进壳聚糖的降解,高浓度的氢离子会抑制降解,即相同条件下在较高浓度酸(>0.23%)中得到的壳聚糖分子量比较低浓度酸(0.23%)中的大。
| 图表编号 | XD00117750500 严禁用于非法目的 |
|---|---|
| 绘制时间 | 2019.12.01 |
| 作者 | 陈声、侯婷婷、江雅婷、李思东、梁丽媚、李永振、陈小娟、张咏诗 |
| 绘制单位 | 广东海洋大学化环学院、广东海洋大学化环学院、广东海洋大学化环学院、广东海洋大学化环学院、广东海洋大学化环学院、中国热点农业科学院农产品加工研究所、中国热点农业科学院农产品加工研究所、广东海洋大学化环学院、广东海洋大学化环学院 |
| 更多格式 | 高清、无水印(增值服务) |
 提示:宽带有限、当前游客访问压缩模式
提示:宽带有限、当前游客访问压缩模式