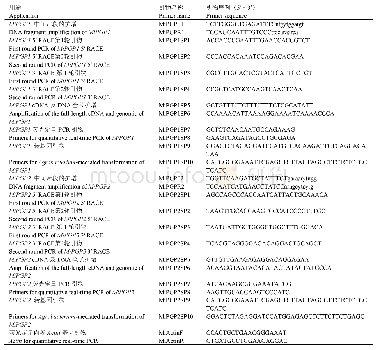
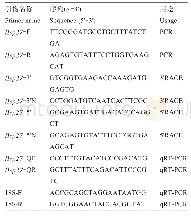
《表1 基因克隆引物及荧光定量引物》
引物名称中含有q PCR的为实时荧光定量引物。
由于GmR47及GmR51具有高度同源性,故采用特异性较高的巢式PCR(Nested-PCR)进行扩增。以NCBI上公布的Williams 82基因组Wm82.a2.v1数据库为参考,利用Primer premier 5软件设计引物(表1)。首先使用引物对GmR47-1和GmR51-1进行第1步PCR,反应体系为50μL,包含酶25μL2×PrimerStar Master Mix(Takara)、上下游引物(浓度为10μmol L-1)各1μL、模板cDNA 1μL、灭菌ddH2O22μL。PCR程序为95℃3 min;98℃10 s,58℃15s,72℃45 s,30个循环;72℃5 min。然后使用引物对GmR47-2和GmR51-2进行第2步PCR,反应体系为50μL,包含酶25μL 2×PrimerStar Master Mix(Takara)、上下游引物(浓度为10μmol L-1)各1μL、模板为第1步PCR产物稀释100倍后取1μL、灭菌ddH2O 22μL。反应程序同上。利用琼脂糖凝胶电泳法检测第2步PCR反应产物,回收条带大小正确的产物。并将回收产物使用T4连接酶连接至T-easy载体pMD20-T,将连接产物转化大肠杆菌感受态DH5α中过夜培养,挑取单克隆,将检测为阳性的单克隆送至通用生物公司测序。
| 图表编号 | XD00112624400 严禁用于非法目的 |
|---|---|
| 绘制时间 | 2019.12.12 |
| 作者 | 向文扬、杨永庆、任秋燕、晋彤彤、王丽群、王大刚、智海剑 |
| 绘制单位 | 南京农业大学大豆研究所、农业部大豆生物学与遗传育种重点实验室、国家大豆改良中心、作物遗传与种质创新国家重点实验室、南京农业大学大豆研究所、农业部大豆生物学与遗传育种重点实验室、国家大豆改良中心、作物遗传与种质创新国家重点实验室、南京农业大学大豆研究所、农业部大豆生物学与遗传育种重点实验室、国家大豆改良中心、作物遗传与种质创新国家重点实验室、南京农业大学大豆研究所、农业部大豆生物学与遗传育种重点实验室、国家大豆改良中心、作物遗传与种质创新国家重点实验室、南京农业大学大豆研究所、农业部大豆生物学与遗传育种重点 |
| 更多格式 | 高清、无水印(增值服务) |
 提示:宽带有限、当前游客访问压缩模式
提示:宽带有限、当前游客访问压缩模式